Tratamiento con inhibidores de PCSK9 en pacientes con enfermedad renal crónica de muy alto riesgo cardiovascular
Los factores de riesgo para la enfermedad cardiovascular son altamente prevalentes en los pacientes con enfermedad renal crónica (ERC), encontrándose entre ellos la dislipidemia 1 . El tratamiento con estatinas ha demostrado disminuir los even- tos cardiovasculares y la mortalidad en pacientes con ERC estadios G3a-G5, por lo que se aconseja su prescripción 2 . Sin embargo, un porcentaje significativo de pacientes no alcanza objetivos terapéuticos o presentan efectos indeseables 2–4 . Los inhibidores de la proproteína convertasa subtilisina/kexina tipo 9 (iPCSK9) pueden suponer una alternativa en el manejo en estos pacientes.
Realizamos un estudio de cohortes retrospectivo de pacientes con ERC que iniciaron tratamiento con iPCSK9 en nuestro centro entre 2016 y 2020. Comparamos las cifras de colesterol total, colesterol ligado a lipoproteínas de baja densidad (c-LDL), triglicéridos y filtrado glomerular estimado (FGe) al inicio del tratamiento y a los 6, 12 y 24 meses. Se evaluó la evolución y aparición de eventos adversos relacionados con el fármaco.
Durante el periodo de estudio se incluyeron 41 pacientes. De ellos, 21 fueron tratados con alirocumab y 20 con evolocumab. Las características basales se recogen en la tabla 1 . Un 51,2% eran hombres con una mediana de edad de 73 a ̃ nos y una mediana de FGe de 46 mL/min/1,73 m2 . Cuatro pacientes tenían un FGe < 30 mL/min/1,73 m2 y uno se encontraba en diálisis peritoneal. El 87,8% habían presentado eventos coronarios. Todos habían recibido previamente estatinas y el 75,1% ezetimiba. El 53,7% de los pacientes iniciaron iPCSK9 por no alcanzar objetivos de c-LDL, mientras que el resto fue por into- lerancia a dosis máximas de estatinas. El seguimiento medio tras el inicio del fármaco fue de 28 meses.

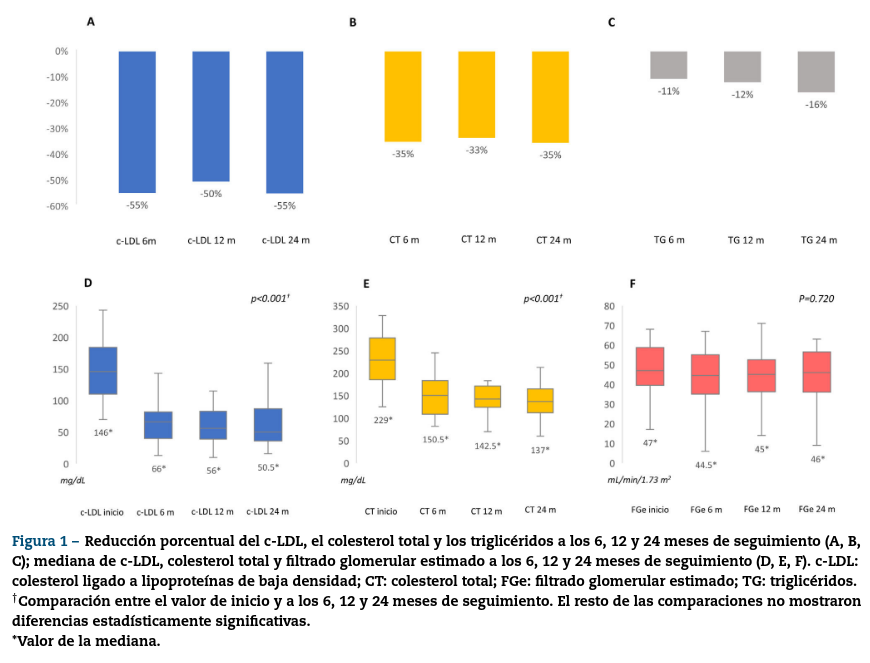
Tras 6 meses objetivamos una mejoría significativa del perfil lipídico, con una reducción del colesterol total de un 35,3% (p < 0,001) y de las cifras de c-LDL de un 54,9% (p < 0,001) permitiendo que el 48,8% de los pacientes alcanzaran obje- tivos de c-LDL por debajo de 55 mg/dL y el 65% por debajo de 70 mg/dL. Dichas diferencias se mantuvieron a lo largo de todo el seguimiento. Los triglicéridos también se redujeron en un 15,8% a los 6 meses (p = 0,019). La función renal se mantuvo estable durante el periodo de estudio (p = 0,720) (fig. 1). No se documentaron eventos adversos relacionados con su prescripción ni abandonos en el tratamiento, y no se reportó ningún evento cardiovascular.
Presentamos una de las series más numerosas que evalúa la efectividad y seguridad de los iPCSK9 en pacientes con ERC en la vida real. Además, el seguimiento analizado es el de más largo plazo descrito hasta ahora. En nuestra experiencia, el c-LDL se redujo más del 50% en los primeros 6 meses de tratamiento, permitiendo que la mitad de los pacientes alcanzasen objetivos terapéuticos rápidamente5. Este dato guarda relevancia ya que, en pacientes en tratamiento con estatinas, un descenso insuficiente de los niveles de c-LDL se relaciona con un mayor riesgo de enfermedad cardiovascular4,5. Un reciente estudio prospectivo que incluye 1.886 pacientes con ERC objetiva una relación lineal entre el c-LDL y la aparición de eventos cardiovasculares, de modo que el riesgo se reduce con niveles de c-LDL < 70 mg/dL6. Estos pacientes que no logran objetivos terapéuticos podrían beneficiarse del uso de iPCSK9. Hasta la fecha disponemos de 2 series retrospectivas en nuestro país que reportan resultados similares7,8. En nuestra cohorte de pacientes, la severidad de la ERC era superior sin que esto afectara la seguridad del tratamiento y sus resultados. Uno de nuestros pacientes se encontraba en diálisis peritoneal, siendo el segundo caso comunicado hasta la fecha9.
Asimismo, reportamos una excelente tolerancia al fármaco. La función renal se mantuvo estable y no se registraron eventos adversos ni abandonos del tratamiento durante el periodo del estudio, evidenciando un perfil de seguridad similar al de la población general10. El desarrollo de nuevos tratamientos efectivos y bien tolerados podría ofrecer beneficios en la reducción de eventos cardiovasculares y mortalidad en nuestros pacientes. Sin embargo, no existen ensayos clínicos que evalúen el uso de los iPCSK9 en pacientes con FGe ≤ 30 mL/min/1,73 m2 y la evidencia es limitada, por lo que su prescripción debe hacerse con cautela. Nuestro trabajo presenta limitaciones, ya que se trata de un estudio de cohortes retrospectivo, con las limitaciones inherentes a su diseño. Asimismo, es una cohorte pequeña y no disponemos de grupo control. Sin embargo, el tiempo de seguimiento es superior al reportado en series previas7–9. Como conclusión, los iPCSK9 son seguros y eficaces en los pacientes con ERC, incluso con FGe ≤ 30 mL/min/1,73 m2. Permiten una mejoría en el control lipídico, manteniendo la función renal estable y con un buen perfil de seguridad. Debido a los aparentes beneficios de estos fármacos en pacientes con ERC, consideramos que se deben diseñar ensayos clínicos que incluyan esta población.
Bibliografía
- Jankowski J, Floege J, Fliser D, Böhm M, Marx N. Cardiovascular disease in chronic kidney disease: Pathophysiological insights and therapeutic options. Circulation. 2021;143:1157-72. https://doi.org/10.1161/CIRCULATIONAHA.120.050686.
- Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2013 clinical practice guideline for lipid management in chronic kidney disease. Kidney Int Suppl. 2013;3:259–305.
- Massy ZA, Ferrières J, Bruckert E, Lange C, Liabeuf S, Velkovski-Rouyer M, et al. Achievement of low-density lipoprotein cholesterol targets in CKD. Kidney Int Rep. 2019;4:1546–54. https://doi.org/10.1016/j.ekir.2019.07.014.
- Weng SF, Akyea RK, Man KK, Lau WCY, Iyen B, Blais JE, et al. Determining propensity for sub-optimal low-density lipoprotein cholesterol response to statins and future risk of cardiovascular disease. PLoS One. 2021;16:e0260839. https://doi.org/10.1371/journal.pone.0260839.
- Grupo de Trabajo de la Sociedad Europea de Cardiología (ESC) y la European Atherosclerosis Society (EAS) sobre el Tratamiento de las Dislipemias. Guía ESC/EAS 2019 sobre el tratamiento de las dislipemias: modificación de los lípidos para reducir el riesgo cardiovascular. Rev Esp Cardiol. 2020;73:403.e1–70. https://doi:10.1016/j.recesp.2019.10.031.
- Lee C, Park JT, Chang TI, Kang EW, Nam KH, Joo YS, et al. Low-density lipoprotein cholesterol levels and adverse clinical outcomes in chronic kidney disease: Results from the KNOW-CKD. Nutr Metab Cardiovasc Dis. 2022;32:410–9. https://doi.org/10.1016/j.numecd.2021.09.037.
- Goicoechea M, Álvarez V, Segarra A, Polaina M, Martín-Reyes G, Robles NR, et al. Perfil clínico de los pacientes tratados con evolocumab en unidades hospitalarias de nefrología en Espa ̃na (RETOSS-NEFRO). Nefrologia. 2022;42:301-10. https://doi.org/10.1016/j.nefro.2021.06.004.
- Escudero Quesada V, Pantoja Pérez J, Castro Alonso C, Osma Capera JV, Valero Antón A, Sancho Clabuig A. Experiencia con inhibidores PCSK9 desde una consulta de Nefrología. Nefrologia. 2022. https://doi.org/10.1016/j.nefro.2022.04.0.
- Rivas Oural A, Astudillo Cortés E, Bande Fernández JJ, Rodríguez Suárez MC, Díaz Corte MC. Tratamiento con alirocumab en paciente en diálisis peritoneal con intolerancia a estatinas. Nefrologia. 2021;21:76–9. https://doi.org/10.1016/j.nefro.2020.04.015.
- Quiroga B, Mu ̃noz Ramos P, Alvarez Chiva V. Efectividad y seguridad del uso de inhibidores de PCSK9 en el tratamiento de la dislipidemia en el paciente con insuficiencia renal. Nefrologia. 2020;40:491–578. https://doi.org/10.1016/j.nefro.2020.04.020.
José Manuel Amaro a, Florentino Villanego a, Javier Naranjo a, Cristhian Orellana a, Luis Alberto Vigara a, Carlos Eduardo Narváez a, Julia Torrado a, Juan Manuel Cazorla a, Claudia Rodríguez b y Auxiliadora Mazuecos a,∗
- Servicio de Nefrología, Hospital Universitario Puerta del Mar, Cádiz, España
- Servicio de Farmacia Hospitalaria, Hospital Universitario Puerta del Mar, Cádiz, España

