Síndrome de Ogilvie: Conceptos actuales en diagnóstico y tratamiento
Resumen
Objetivo: Revisión de la literatura y actualizar los conceptos en la etiopatogenia, diagnóstico y tratamiento del síndrome de Ogilvie (SO)/distensión masiva aguda del colon derecho. Para saber si su origen proviene del colon o de las patologías asociadas al mismo. Material: Se revisaron los artículos publicados hasta la fecha donde analizamos la edad, sexo, condición clínico-patológica, tratamientos previos y definitivos. Resultados: La patología más frecuente casuísticamente en todos fue la endocrina y metabólica (Diabetes, desequilibrio hidroelectrolítico e hipotiroidismo). Le siguió la postquirúrgica sobre todo la cirugía ortopédica-traumatológica oncológica, renal, gastroenterológica y en algunos casos: la ginecológica, neurológica, infecciosa, cardiovascular, farmacológica y tóxica. Discusión: El síndrome de Ogilvie no por ser una entidad rara, debe escapar al médico de primer contacto, que por experiencia debemos hacer un diagnóstico diferencial sobre todo en el Servicio de Urgencia. Es importante realizar el diagnóstico lo antes posible para poder instalar el tratamiento adecuado especialmente en el paciente crítico. El tratamiento multidisciplinario debe ser la regla. Conclusiones: Los pacientes con este síndrome considerando su edad y sexo, después de tomarle la placa de Rx de abdomen y ser diagnosticados podemos concluir que su origen está en el colon, ya que así lo demuestra la fisiopatogenia y deben ser tratados dependiendo de su estado mórbido con un esquema de tratamiento instituido en su hospital; si esta condición es inicial o de primera vez se aplicaran las medidas básicas para corregir el desequilibrio hidroelectrolítico, control de la glucosa e infección; si sólo hay dilatación del asa intestinal las sondas nasogástricas y rectal son de mucha ayuda. Dependiendo de la evolución se desarrollará el algoritmo de tratamiento institucional; en nuestro caso es el que mencionamos o el propuesto en muchos estudios a nivel internacional. Siempre vigilando la evolución del paciente y de acuerdo a la buena, regular o mala respuesta se agotaran todas las medidas propuestas.
Palabras clave: Síndrome de Ogilvie, distensión masiva aguda del colon derecho.
INTRODUCCIÓN
El síndrome de Ogilvie (SO) o pseudoobstrucción aguda del colon fue descrito en 1948 y publicado en la British Medical Journal por el doctor chileno William Heneage Ogilvie, nacido en Valparaíso el 14 de julio de 1887. Antes de Ogilvie, en 1896 Murphy4 describió por primera vez esta entidad durante una laparotomía, cuando encontró una distensión del colon proximal secundaria que él consideró un «espasmo del intestino». Había postulado que (como lo haría Ogilvie 50 años más tarde) el síndrome se caracterizaba por una dilatación masiva y aguda del colon, especialmente del lado derecho; varios reportes en la literatura señalan que afecta hasta el ángulo esplénico.3,4 Es una entidad clínica rara, predomina en pacientes del sexo masculino, generalmente se presenta en enfermos hospitalizados con alguna patología médica o quirúrgica grave y un porcentaje bajo en pacientes ginecoobstétricas2,3 (Cuadro I).

Los médicos de Urgencia, Medicina Interna y Ginecoobstetricia deben tener en mente esta patología y estar al tanto de su aparición, ya que si no se trata al inicio del cuadro clínico confirmado con estudios de laboratorio y gabinete, puede complicarse con perforación, peritonitis y muerte. Los índices de morbilidad varían en la literatura: entre más temprano se inicie el tratamiento, el porcentaje de curación es mayor hasta un 80%, si se emplean las medidas generales para este padecimiento, un esquema de fármacos procinéticos (Cuadro II) de la pasada y nueva generación,10 (mesaprida, itoprida, cinetaprida, etc.) y antibióticos según los resultados del laboratorio, por ejemplo eritromicina más neostigmina como control. Aún así, presentan un porcentaje de recidiva del 6-14%, de éstos sólo 20% llegan a ser quirúrgicos y son aquellos que recidivaron y/o llegaron con diagnóstico tardío o sin respuesta al tratamiento médico agresivo e intensivo de la descompresión con aplicación de sondas nasogástrica y rectal, corrección del desequilibrio hidroelectrolítico, control de cualquier anormalidad metabólica de fondo y descompresión endoscópica que por sus resultados buenos a excelentes (66-90%) compiten favorablemente contra una cirugía mayor, con mortalidad del (25 al 50%) y morbilidad del (3%).

DEFINICIÓN
El SO es una entidad nosológica heterogénea de fisiopatología aún no definida, asociada a diversas condiciones médicas o quirúrgicas que se caracteriza por una dilatación aguda del colon, segmentaria o total que en ausencia de obstrucción mecánica se le ha denominado pseudoobstrucción.
SINÓNIMOS
Obstrucción colónica falsa (Dunlop, 1945), pseudomegacolon (Creech, 1950), megacolon adquirido (Drye & Pirkey, 1950), pseudoobstrucción del colon (Dudley et al, 1958), íleo adinámico del Colon (Morton et al, 1960), megacolon del adulto sin obstrucción (Melamed et al, 1960), íleo paralítico del colon (Byrne et al, 1960), obstrucción idiopática del intestino grueso (RothwellJackson, 1963), obstrucción funcional del colon (Melamed & Kubian, 1963) e íleo hipocalémico del colon (Muggia, 1972).5
ETIOLOGÍA
Su etiología es desconocida,1,6 dado que este síndrome se asocia a múltiples entidades patológicas, quirúrgicas y farmacológicas, es probable que existan varios mecanismos fisiopatológicos. El mismo Ogilvie señala la hipótesis de un desequilibrio autonómico del control intrínseco como base del síndrome, confirma este enunciado al obtenerse un alivio sintomático por medio del bloqueo adrenérgico seguido por la estimulación colinérgica o por el uso de neostigmina sola.
FISIOPATOLOGÍA
Aunque el SO no tenga una etiología bien sustentada, y otros autores la consideren como desconocida,21 se presume un disbalance entre la inervación simpática y parasimpática del colon, su dilatación es producida por factores no mecánicos. Este concepto de que la pared del colon y recto puede relajarse en respuesta a estímulos fisiológicos y farmacológicos, propuesto por el mismo Ogilvie, explica un desequilibrio autonómico del control intrínseco como base del síndrome. Esta hipótesis se ha comprobado al obtener un alivio sintomático por medio de un bloqueo adrenérgico conseguido por la estimulación colinérgica o por el uso de neostigmina sola (Figura 1).
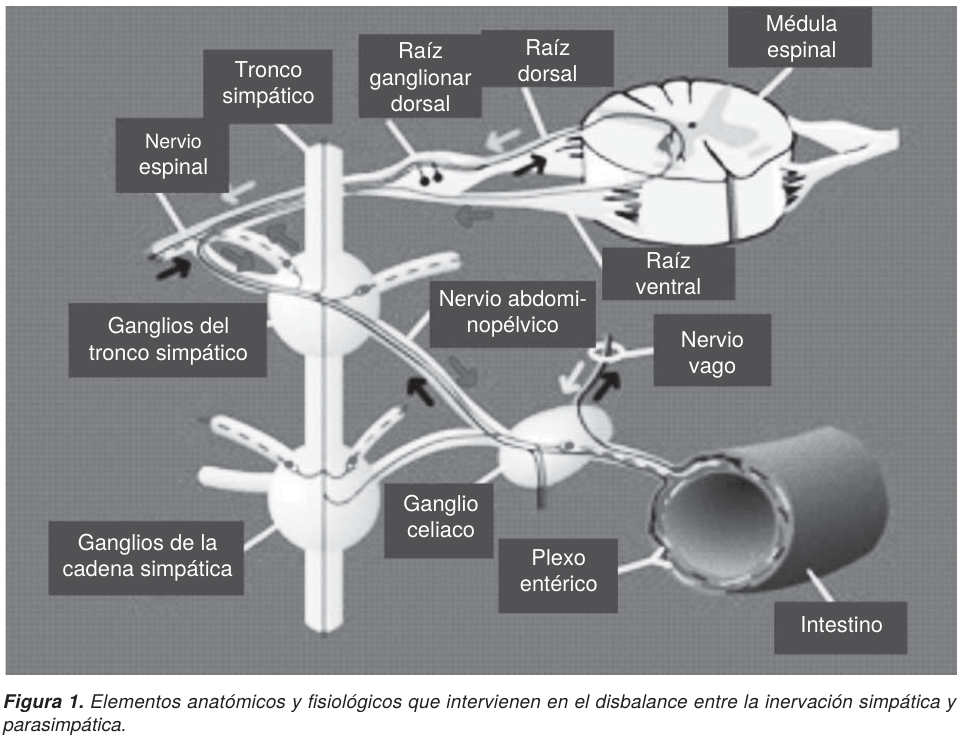
CUADRO CLÍNICO
Se caracteriza por una distensión abdominal moderada a severa acompañada de disnea, dolor tipo cólico en hipogástrio, puede cursar con estreñimiento y/o dificultad para canalizar gases y en casos raros puede haber diarrea. En la exploración del abdomen existe timpanismo generalizado, los ruidos peristálticos pueden estar disminuidos o ausentes. Al principio del cuadro clínico no hay signos peritoneales y el recuento de leucocitos es normal, sobre todo en paciente con una evolución progresiva, hospitalaria (3 a 7 días); secundaria a una intervención quirúrgica o tratamiento médico. También hay una forma de presentación súbita (24 a 48 h); el desequilibrio electrolítico se acompaña en esta fase con náusea y vómito, además existen signos de irritación peritoneal por perforación, posibilidad de neumoperitoneo y peritonitis. Es importante tener los antecedentes personales patológicos del paciente y causas que con mayor frecuencia se asocian a este síndrome, para tratar de evitar una confusión diagnóstica y provocar una iatrogenia (Cuadro III).
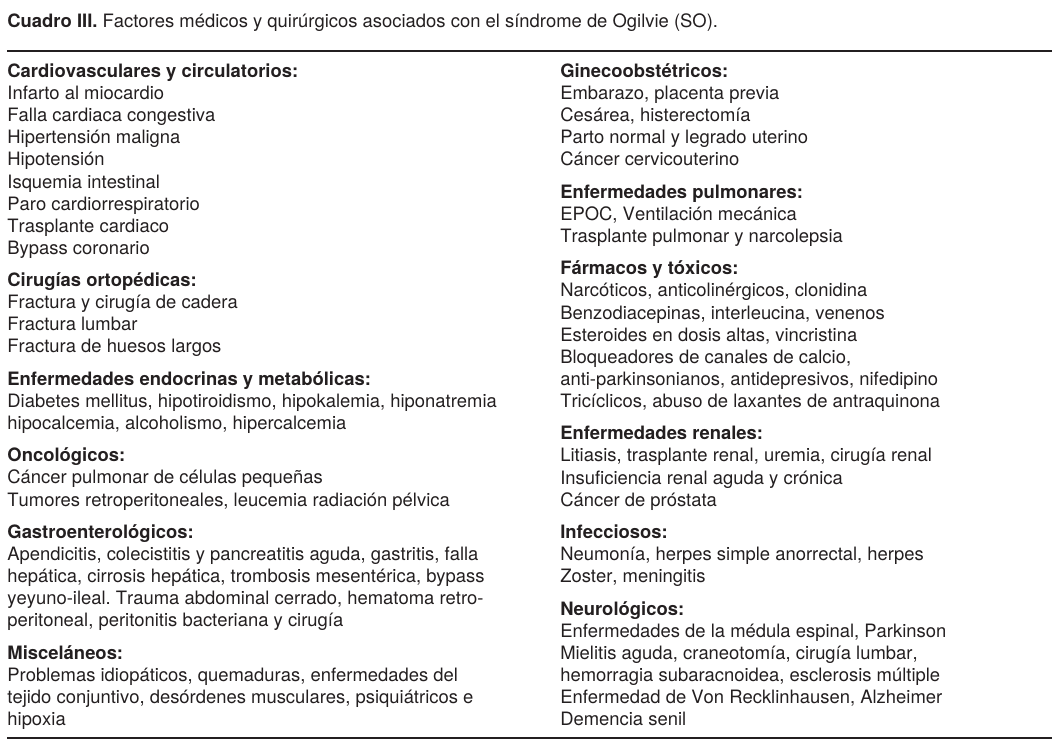
DIAGNÓSTICO
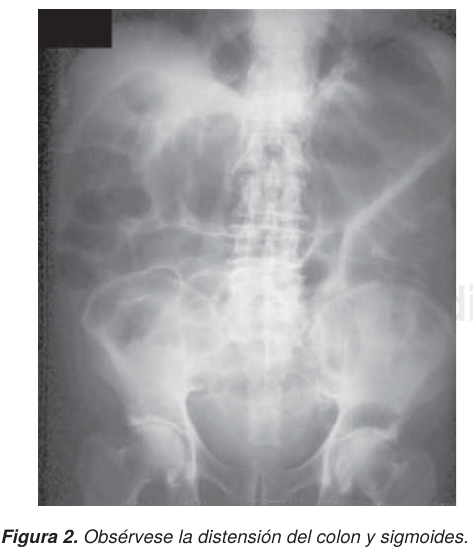
El diagnóstico del síndrome de Ogilvie debe sospecharse en pacientes hospitalizados, con o sin cirugía previa o con alguna de las múltiples entidades a las que se asocia. La radiografía simple de abdomen (Figura 2); es el estudio de gabinete esencial para el diagnóstico, la cual muestra como característica una dilatación-distensión gaseosa masiva del colon hasta el ángulo esplénico, distensión moderada del intestino delgado, ausencia de niveles y edema en la pared. El enema baritado a baja presión permite junto con la colonoscopia determinar la ausencia de lesión en la luz del colon. Si el cuadro clínico es de presentación paulatina (3 a 7 días), se pueden para tomar radiografías simples seriadas de abdomen para valorar el posible aumento de volumen del colon derecho. Las técnicas de la colonoscopia para el diagnóstico y tratamiento han sido modificadas de acuerdo a los casos. La tomografía axial computada (TAC), recurso de imagen más detallado para el diagnóstico, y la radiología intervencionista han revolucionado el tratamiento médico para el SO, sin recurrir a la cirugía, aunque ésta se tenga que realizar sobre todo en los casos complicados o recidivantes.
TRATAMIENTO
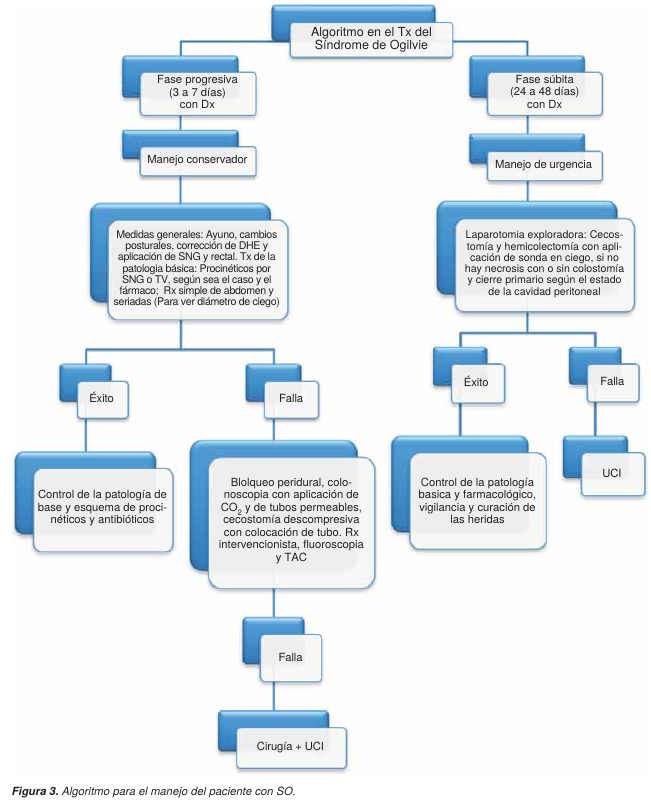
El tratamiento médico general del SO comprende diversas alternativas terapéuticas (Figura 3), desde medidas generales poco invasivas hasta la utilización de la descompresión colónica por colonoscopia y cirugía. Frecuentemente se inicia con ayuno (reposo intestinal), sonda nasogástrica y rectal, enemas evacuantes, cambios posturales, tratamiento de la enfermedad de origen, reposición hidroelectrolítica y supresión de drogas potencialmente implicadas en el desarrollo del síndrome.9,10-15 El tratamiento farmacológico más recomendado actualmente en SO es para corregir el desequilibrio del sistema autónomo de la motilidad colónica,5,10-12,16,19 basados en este hecho, se han utilizado actualmente la cinitaprida, la mesaprida y la itoprida,34 por su acción procinética sobre el colon, y su potente acción selectiva sobre los receptores 5-HT4, 5-HT2 y D2 produciendo liberación de acetilcolina en los plexos mientéricos (Cuadro IV).

La utilización de naloxona, un antagonista opioide está justifi cada en pacientes que han recibido analgésicos opiáceos. La anestesia epidural con bupivacaína16 se sustenta teóricamente en que el bloqueo simpático esplácnico aumenta el tono y la motilidad colónica. También se ha empleado el tratamiento combinado de bloqueo gangliónico con guanetidina seguido de estimulación colinérgica usando neostigmina con resultados positivos.23,24 Hay reportes de pacientes tratados con prostaglandinas con buenos resultados.22 La eritromicina un antibiótico macrólido agonista de la motilina con efecto sobre el músculo liso gastrointestinal, se ha usado en forma limitada en este síndrome.
CONCLUSIONES
El tratamiento farmacológico de series reportadas en la literatura con múltiples esquemas, donde se ha llehic.org.mx gado a establecer recomendaciones para la realización de estudios randomizados, controlados no sesgados para conocer el riesgo/beneficio de cada paciente. La descompresión colónica endoscópica fue introducida en 1977 por Kukora y Dent,33 publicaron una serie de seis pacientes con SO que fueron tratados con descompresión del colon utilizando un endoscopio, en cinco de seis pacientes el procedimiento fue exitoso, dando lugar a que la colonoscopia, se convirtiera en uno de los procedimientos más utilizados en el manejo de estos pacientes; con la única contraindicación, en los casos de isquemia de la mucosa y peritonitis. La limpieza mínima Este del colon documento en ciertos es elaborado casos con 1,000 por Medigraphic mL de solución jabonosa con el objeto de diluir las heces y puedan ser aspiradas fácilmente, el procedimiento debe hacerse insuflando una cantidad mínima de aire a las asas intestinales, para evitar una perforación; últimamente se ha utilizado el CO2 que se absorbe rápidamente, tiene un efecto vasodilatador y disminuye la posibilidad de isquemia y perforación.
Sin embargo, siempre existe la posibilidad de una perforación.5,17,18-27 Debido a las recidivas con la colonoscopia descompresiva, se han propuesto varias modificaciones al procedimiento: 1) la colonoscopia con doble canal de trabajo y colocación del tubo de drenaje fenestrado que se introduce utilizando las pinzas de biopsia o el asa de polipectomía;25 2) colonoscopia con canal de trabajo único y colocación de guía cubierta por teflón con paso posterior de un tubo fenestrado a través de la guía, y 3) colonoscopia con un sobretubo fenestrado.17 En la técnica de descompresión colonoscópica con tubo de drenaje, lo ideal es dejar el catéter en ciego, sin embargo, este objetivo es un reto para el endoscopista debido a que se realiza el procedimiento en un colon no preparado y en un paciente habitualmente grave. Otra alternativa reciente es usar un stent de metal expandible para la obstrucción no complicada.33 También se ha demostrado que la sonda de drenaje colocada en el sitio proximal al ángulo esplénico ofrece iguales resultados terapéuticos.30 La recomendación de la cirugía se basa en los cambios isquémicos en la pared cecal que inicia en la serosa y progresa a la mucosa, de tal forma que la presencia de isquemia de la mucosa debe interpretarse como una afección transmural con alto riesgo de perforación. La cirugía como se ha señalado anteriormente es necesaria después de la recidiva o complicación al efectuar la descompresión.
La cecostomía percutánea es un método eficaz descrito como alternativa de tratamiento en pacientes con SO. Este tratamiento se reserva para pacientes en quienes no fue posible practicar una colonoscopia descompresiva por dificultades técnicas o que no han mostrado mejoría después de ésta. Este procedimiento es realizado por un radiólogo intervencionista. Se utiliza un abordaje de tipo transperitoneal o retroperitoneal guiado por tomografía axial computada; 30,31 se ha sugerido que el abordaje retroperitoneal puede tener algunas ventajas, como la retención en el retroperitoneo del contenido cecal en caso de fuga, evitando la peritonitis; sin embargo, en los casos reportados en la literatura donde se ha utilizado un abordaje transperitoneal, la peritonitis no ha representado una complicación importante pero la presencia de heces en retroperitoneo puede causar una fascitis infecciosa. 20,29,32 Los estudios anatómicos en cadáveres sugieren que el abordaje retroperitoneal es muy difícil, esto debido a la extensión posterolateral del peritoneo y la sobreposición lateral y posterior del hueso iliaco.20 La cecostomía percutánea tiene la desventaja de que no precisa el grado de necrosis de la mucosa intestinal ni la presencia de perforaciones.
El sistema coaxial de tres componentes guiado por fluoroscopia es otra de las técnicas utilizadas por los radiólogos para el manejo del SO. Este procedimiento surgió de la idea que la falla de los tubos rectales se debía a que éstos eran muy cortos. Este sistema es una modificación del catéter tradicional coaxial angiográfico. Incluye un catéter rectocolónico externo, un catéter guiado interno y una guía central de alambre central, que se introduce a través del recto y con el uso de fluoroscopia puede ser guiado hasta el colon proximal, este método también tiene sus limitantes y al final no valora el estado de isquemia de la mucosa y su principal complicación es la hemorragia y perforación.25
Tratamiento quirúrgico para el SO. Las modalidades son: cecostomía descompresiva, colectomía y/o colostomía, consisten en efectuar una laparotomía exploradora con objeto de evaluar las condiciones y complicaciones del colon (isquemia, necrosis, perforación, abscesos y peritonitis). Cuando el colon no tiene datos de isquemia o perforación, el procedimiento de elección es la colocación de un tubo de cecostomía. Cuando el estado del colon demuestra un grado importante de isquemia, necrosis y perforación la resección colónica será la propuesta y el cirujano decidirá de acuerdo a su experiencia y al estado de la cavidad peritoneal, si el cierre es primario con o sin protección de una colostomía. La laparoscopia como método de diagnóstico y tratamiento en pacientes con SO, valora el grado de visibilidad y de lesión del intestino. Si durante la laparoscopia se encuentra un ciego con necrosis extensa, se realiza laparotomía y resección intestinal. Si los cambios de isquemia son mínimos, se coloca una sonda en ciego o se realiza la cecostomía por laparoscopia, lo que evita las complicaciones de la cirugía convencional.26
Las recidivas del SO en pacientes tratados por cirugía es prácticamente «nula»,28 sin embargo la morbimortalidad de los procedimiento con cecostomía, resección intestinal y/o colostomía oscila del 20 al 57%.12 La infección de la herida, hernia incisional, prolapso cecal con infarto y eventración son las complicaciones más frecuentes.12
DIAGNÓSTICO DIFERENCIAL
Megacolon adquirido (relacionada con estreñimiento)
Vólvulo colónico (ciego-sigmoides)
Megacolon tóxico amibiano, EII (CUCI y CROHNS)
Colitis infecciosas
Colitis seudomembranosa
Enfermedad de Chagas
Megacolon idiopático
BIBLIOGRAFÍA
- Dorudi S, Berry AR, Kettlewell MG. Acute colonic pseudo-
obstruction. Br J Surg 1992; 79: 99-103. - Ávalos J, León C, Migueles C. Síndrome de Ogilvie ¿Qué
hay de nuevo? Rev Child Cir 2001; 53: 220-225. - Quintero S, Chafeiro VM, Valdovinos D. Síndrome de
Ogilvie o pseudo-obstrucción colónica aguda. Conceptos
actuales en diagnóstico y tratamiento. Rev Gastroenterol
Méx 1997; 62: 119-1. - Cárdenas de la MR, Cárdenas G, Heredia C, Pizarro P.
Manejo del síndrome de Ogilvie. Rev Chil de Cir 2004;
56: 103-106. - Vanek VW, Al-Salti M. Acute pseudo-obstruction of the
colon (Ogilvie’s syndrome). Dis Colon Rectum An Analysis
of 400 cases 1986; 29: 203-209. - Bannura G, Portalier P. Pseudoobstrucción aguda del
colon (Síndrome de Ogilvie). Rev Chil Cir 1994; 46: 265-
271. - Laine L. Management of acute colonic pseudo-obstruc-
tion. NEJM 1999; 341: 192-203. - Zepeda J, Madrigal I, Naranjo E, Hernández K. Síndrome
de Ogilvie. A propósito de un caso. Rev Fac Med UNAM
2005; 48: 131-133. - Vantrappen G. Acute colonic pseudo-obstruction. Lancet
1993; 341: 152-153. - Walwaikar PP, Kulkarni SS, Bargaje RS. Evaluation of
new gastro-intestinal prokinetic (ENGIP-II) study. J Indian
Med Assoc 2005; 103: 708-9. - Olgivie WH. Large intestine colic due to sympathetic de-
privitation. Anew clinical syndrome. BMJ 1948; 2: 671-3. - Hart MB, Rosenmurgy AS. Cecal pseudo-obstruction (early
therapy should be nonoperative). Am Surg 1989; 56: 43-6. - Nanni G, Garbini A, Luchetti P, Ronconi P, Castagneto M.
Ogilvie’s syndrome (Acute colonic pseudo-obstruction).
Dis Colon Rectum 1982; 25: 157-166. - Low GC, Fairley NH. Fatal perforation of the cecum in a
case of sprue. BMJ 1934; 2: 678. - Gifford RM. Ogilvie’s syndrome: A true definition. Arg Surg
1987: 122-958. - Lee JT, Taylor BM, Singleton BC. Epidural anesthesia for
acute pseudo-obstruction of the colon (Ogilvie’s syndro-
me). Dis Colon Rectum 1988; 31: 686-91. - Harig JM, Fumo DE, Loo FD et al. Treatment of acute
nontoxic megacolon during colonoscopy: tube placement
versus simple descompression. Gastrointest Endosc
1988; 34: 23-7. - Nakhgevany KB. Colonoscopy descompression of the
colon in patients with Ogilvie’s syndrome. Am J Surg
1984; 148: 317-320. - Spira IA, Rodríguez R. Pseudo-obstruction of colon. Am
J Gastroenterol 1976; 65: 397-408. - Van Sonnenberg E, Varney RR, Casola G et al. Percuta-
neous cecostomy for Ogilvie’s syndrome: laboratory obser-
vation and clinical experience. Radiology 1990; 175: 679-82. - Montero LC, Hormeño BRM, González ME, Gordillo MB.
Síndrome de Ogilvie o pseudobstrucción aguda del colon,
una causa rara de abdomen. A propósito de un caso.
Anales de Médicina Interna 2006; 23: 100-104. - Post AB, Falk GW, Bukowski RM. Acute colonic pseudo-
obstruction associate with interleukin-2 therapy. Am J
Gastroenterol 1991; 86: 1539-41. - Kukora JS, Dent TL. Colonoscopy descompression of
massive nonobstructive cecal dilatation. Arch Surg 1977;
112: 512-7. - Hutchinson R, Griffiths C. Acute colonic pseudo-obstruc-
tion: a pharmacological approach. A Coll Surg Engl 1992;
74: 364-7. - Bender GN, Do-Dai D, Briggs LM. Colonic pseudo-obs-
truction: descompression with tricomponent coaxial system
under fluoroscopic guidance. Radiologic 1993: 395-8. - Uh QY, Way L. Diagnostic laparoscopy and laparoscopy
cecostomy for colonic pseudo-obstruction. Dis Colon
Rectum 1993; 36: 65-70. - Geelhoed GW. Colonic pseudo-obstruction in surgical
patients. Am J Surg 1985; 149: 258-65. - Adam JT. A dynamic ilium of the colon. Arch Surg 1974;
109: 503-7. - Haaga JR, Ronald JB, Zollinger RM. CT-Guided percu-
taneous catheter cecostomy. Gastrointest Radiol 1987;
12: 166-68. - Lowman RM, Davis L. An evaluation of cecal size in
impeding perforation of the cecum. Surg Ginecol Obstet
1956; 103: 711-8. - Johnson CD, Rice RP, Kelvin FM, Foster WL, Williford
ME. The radiologic evaluation of gross cecal distension:
emphasis on cecal ileus. AJR 1985; 145: 1211-7. - Casola G, Withers C, VanSonnenberg E, Herba MJ, Saba
RM, Brown RA. Percutaneous cecostomy for descom-
pression of the massively distended cecum. Radiology
1986; 158: 793-4. - Baron TH, Dean PA, Yates MR III et al. Expandable metal
stents for the treatment of colonic obstruction: Techniques
and outcomes. Gastrointest Endosc 1998; 47: 277. - Walwaikar PP, Kulkami SS, Bargaje RS. Evaluation of
new gastro-intestinal prokinetic (ENGIP) study. J Indian
Med Assoc 2005; 103: 708-9.
Autores
Gabriel Bucio Velázquez,*
Salvador López Patiño,**
Luisa Dayana Bucio
Ortega***
*Director de la Unidad de Coloproctología del Bajío, Torre Médica de Celaya, Guanajuato.
** Director del Laboratorio de Patología y Citología del Centro de Diagnóstico Médico y Hospital Médica Avanzada Celaya (MAC).
*** MPSS.
Revista Mexicana de Coloproctología Vol. 17
Dr. Gabriel Bucio Velázquez

